De simpelste proefjes die met elektriciteit te maken hebben gaan over lading. Wanneer je een ballon langs een wollen trui wrijft, krijgt deze elektrische lading. Als je de ballon daarna bij iemands haar houdt, zal de ballon aan het haar ‘trekken’ waardoor het omhoog zal gaan staan.
Bewegende lading
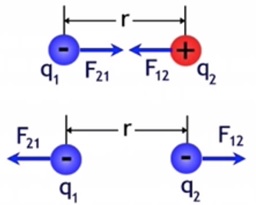
Er zijn twee verschillende soorten lading. Deze worden positieve en negatieve ladingen genoemd. Door het wrijven wordt de ballon negatief geladen. De elektrische kracht die tussen twee voorwerpen werkt kun je dan verklaren. De kracht tussen twee gelijke ladingen (positief en positief, negatief en negatief) is afstotend, en tussen twee ongelijke ladingen (positief en negatief) aantrekkend. Het symbool van lading is Q of q en de eenheid is coulomb, afgekort C.
Niet alle voorwerpen zijn elektrisch geladen. Als voorwerpen evenveel negatieve als positieve lading bevatten zijn ze neutraal geladen. In dat geval kan er ook een aantrekkende elektrische kracht werken. Als je de negatief geladen ballon in de buurt van je haar houdt, trekt de ballon aan je haar, terwijl dat neutraal geladen is. Blijkbaar heeft de aanwezigheid van een elektrische lading invloed op de lading van andere voorwerpen in de omgeving. Dit heet influentie.
De negatief geladen ballon trekt aan de positief geladen deeltjes in het haar . Tegelijkertijd stoot de negatief geladen ballon negatief geladen deeltjes af. Hierdoor verplaatst de negatieve lading van de ballon af en wordt de positieve lading door de ballon aangetrokken.
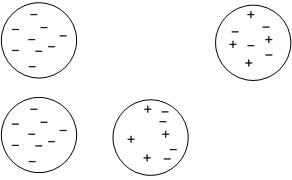
Een neutrale lading ondervindt een aantrekkende kracht door influentie.
Lading meten
Er zijn verschillende manieren om lading te meten. Een daarvan is de elektrometer. Deze apparaten kunnen zeer nauwkeurig de hoeveelheid lading meten. Een ander apparaat is de elektroscoop. Deze bestaat uit een metalen buis die eindigt in twee dunne plaatjes. Als er een lading aanwezig is aan de bovenkant bij de ronde bol, gaat de lading zich in de buis verdelen. De negatieve lading gaat door een positieve lading richting de bol, en door een negatieve lading richting de plaatjes. Hierdoor krijgen de metalen plaatjes allebei dezelfde lading. Dit zorgt ervoor dat ze elkaar afstoten. De grootte van de afstoting van de plaatjes is een maat voor de grootte van de lading.

Een elektroscoop.
Elektronen, protonen en neutronen
Ladingsverschillen worden veroorzaakt door de aanwezigheid of afwezigheid van de negatieve elektronen. Een atoom bestaat uit een kern met neutronen en protonen, die omcirkelt worden door elektronen. De elektronen zijn relatief zwak gebonden aan de kern. Als je bijvoorbeeld een ballon langs een wollen trui wrijft, springen de elektronen van de atomen in de trui over op de atomen in de ballon.
In de kern is ook lading aanwezig. Die zorgt ervoor dat de elektronen bij de kern blijven. De lading in de kern is positief en wordt veroorzaakt door de protonen. Neutronen zijn zoals de naam doet vermoeden neutraal geladen. De afstotende kracht van de protonen onderling wordt opgeheven door de kernkracht tussen de protonen en neutronen.
De lading van één proton is de kleinst mogelijke lading die in de natuur voorkomt. Verder is dit een vaste waarde: elk proton heeft dezelfde lading. Deze lading wordt het elementair ladingsquantum genoemd. Het symbool hiervan is e en de waarde is 1,60218 × 10−19 C. Normaal bevat een atoom evenveel protonen als elektronen, waardoor de netto lading neutraal is. Als er meer of minder elektronen dan protonen zijn, is het atoom een ion geworden.
Voorbeeld 1 Een kam
Een kam heeft een lading van −3,0 μC. Bereken hoeveel extra elektronen er zijn.
De lading van de kam is −3,0 × 10−6 C. De lading van één elektron is −1,60 × 10−19 C.
Dit geeft: (−3,0 × 10−6) / (−1,60 × 10−19) = 1,9 × 1013
Er zijn dus 1,9 × 1013 extra elektronen.
Isolatoren
Het is bekend dat lading zich beter kan verspreiden in sommige stoffen dan in andere. Dit gaat dan over vrije elektronen. Als deze verplaatst worden, nemen ze de negatieve lading met zich mee. Stoffen waarin elektronen zich minder goed of helemaal niet kunnen bewegen worden isolatoren genoemd. Lading kan zich niet of nauwelijks door een isolator verplaatsen en er zal dus geen stroom door gaan lopen. Voorbeelden van isolatoren zijn plastics, hout, rubber en glas.
Geleiders
Een geleider is een stof waar lading zich goed door kan verplaatsen. In vrijwel alle metalen kunnen elektronen vrij bewegen. Lading kan zich daarom makkelijk door metalen verplaatsen en metalen worden daarom toegepast bij verschillende elektrische apparaten.
Sommige vloeistoffen kunnen geleiden. Dit is het geval wanneer er een zout in opgelost is. Een zout bestaat namelijk uit ionen. Dit zijn atomen die een (aantal) elektron(en) te veel of te weinig hebben, waardoor ze positief of negatief geladen zijn. Een voorbeeld is het menselijk lichaam: dit is geleidend door opgeloste zouten in de vele vloeistoffen zoals bloed of weefselvocht.
Gassen kunnen ook geleiden, maar alleen onder bijzondere omstandigheden. Normaal gesproken zijn gassen neutraal omdat ze uit moleculen bestaan. Soms gebeurt het echter dat een elektron van zo’n molecuul wordt afgestoten. Hierdoor ontstaan ionen. Dit wordt ook wel ionisatie genoemd. Dit kan ook op kunstmatige manier bereikt worden door gasmoleculen te beschieten. Dit gebeurt in tl-buizen, natriumlampen en neonbuizen.
Als er ionisatie van de gasmoleculen in de lucht plaats vindt, kan er ontlading optreden. De bliksem die bij onweer ontstaat is hier een voorbeeld van. Door complexe processen ontstaan er ladingsverschillen in de wolken. De ladingsverschillen worden opgeheft door een stroom van geladen deeltjes in de lucht, waarbij vonken in de vorm van bliksem ontstaan. Door het opwarmen en afkoelen van de lucht ontstaat er een typisch geluid: donder.
Verder zijn er ook nog halfgeleiders. Dit zijn stoffen die onder bepaalde omstandigheden geleiders zijn, en onder weer andere omstandigheden isolatoren zijn. Voorbeelden zijn germanium en silicium.
Samenvatting
- Het symbool van lading is Q of q en de eenheid is coulomb, afgekort C.
- Elektrische lading is positief of negatief. Gelijke ladingen stoten elkaar af, ongelijke ladingen trekken elkaar aan
- Neutrale voorwerpen hebben geen lading. Door influentie kunnen ze alsnog een aantrekkende kracht ondervinden
- Lading kun je meten met een elektrometer of elektroscoop.
- Een atoom bestaat uit negatief geladen elektronen en een positieve kern, die uit positieve protonen en neutronen bestaat.
- De lading van een elektron en proton zijn altijd hetzelfde, alleen tegengesteld. De grootte is het elementair ladingsquantum.
- Geleiding heeft te maken met de aanwezigheid van vrije elektronen.
- In een isolator kan lading niet bewegen door gebrek aan vrije elektronen.
- Geleiders kunnen metalen, vloeistoffen met opgeloste zouten of gassen waarin ionisatie plaats vindt zijn.
- Halfgeleiders zijn onder bepaalde omstandigheden geleiders of isolatoren.
Opdrachten
Opdracht 1 :: Juist of onjuist?
Geef bij de onderstaande beweringen aan of deze juist of onjuist is.
1 Een elektron heeft de tegenovergestelde lading van een waterstofkern.
2 Een negatief geladen voorwerp kan een neutraal voorwerp afstoten.
3 Een ion is een atoom dat een of meerdere elektronen heeft afgestaan of opgenomen.
4 In een metaal zijn de ionen verantwoordelijk voor de geleiding.
Opdracht 2 :: Elektroscoop
Een elektroscoop heeft doordat hij contact heeft gemaakt met een negatief geladen voorwerp een lading van 9,4 × 10−6 C. De elektroscoop wordt ontladen door contact met een staafje ijzer. Hierbij springt de lading over op het staafje. Bereken hoeveel procent de massa toe neemt door het overspringen van de lading. Het staafje woog voordat het lading kreeg 5,0 g.
Elektrische ladingen > Elektrische kracht